更新于:2024-05-08

Jiangsu Alphamab Biopharmaceuticals Co., Ltd
更新于:2024-05-08
概览
标签
肿瘤
消化系统疾病
皮肤和肌肉骨骼疾病
双特异性抗体
ADC
纳米抗体
疾病领域得分
一眼洞穿机构专注的疾病领域
暂无数据
技术平台
公司药物应用最多的技术
暂无数据
靶点
公司最常开发的靶点
暂无数据
| 排名前五的药物类型 | 数量 |
|---|---|
| ADC | 6 |
| 单克隆抗体 | 6 |
| 双特异性抗体 | 3 |
| 纳米抗体 | 1 |
| 抗体 | 1 |
关联
18
项与 江苏康宁杰瑞生物制药有限公司 相关的药物靶点 |
作用机制 PDL1抑制剂 |
原研机构 |
最高研发阶段批准上市 |
首次获批国家/地区 中国 |
首次获批日期2021-11-24 |
作用机制 CTLA4抑制剂 [+1] |
在研机构 |
原研机构 |
在研适应症 |
最高研发阶段临床3期 |
首次获批国家/地区- |
首次获批日期- |
靶点 |
作用机制 HER2拮抗剂 |
在研机构 |
原研机构 |
最高研发阶段临床3期 |
首次获批国家/地区- |
首次获批日期- |
49
项与 江苏康宁杰瑞生物制药有限公司 相关的临床试验Phase I/II Study to Assess the Safety, Tolerability, Pharmacokinetics and Efficacy of JSKN033 in Patients With Advanced or Metastatic Solid Malignant Tumors
This study is an open-label, multicenter, first-in-human, Phase I/II (dose escalation and dose expansion) study to evaluate the safety, tolerability, PK, immunogenicity and efficacy of JSKN033 in patients with advanced unresectable or metastatic solid malignant tumors that are expected to be HER2 expression (IHC ≥ 1+).
开始日期2024-01-18 |
申办/合作机构 |
A Phase 3, Multicenter, Randomized, Open-Label, Active-Controlled Trial Of JSKN003 Versus Treatment Of Physician'S Choice For HER2-low, Unresectable and/or Metastatic Breast Cancer Subjects
This study is a randomized controlled, open-label, multicenter phase III clinical study evaluating the efficacy and safety of chemotherapy selected by investigator JSKN003 s in subjects with recurrent or metastatic breast cancer who have previously failed first- or second-line chemotherapy in subjects with recurrent or metastatic breast cancer who have failed prior first- or second-line chemotherapy.
The study planned to enroll 400 subjects in a 1:1 ratio and stratified block randomization method assigned to:
Experimental group: JSKN003 monotherapy
Control group: investigator's chosen chemotherapy drug (capecitabine, gemcitabine, vinorelbine, docetaxel, albumin-bound paclitaxel, or eribulin) monotherapy
The study planned to enroll 400 subjects in a 1:1 ratio and stratified block randomization method assigned to:
Experimental group: JSKN003 monotherapy
Control group: investigator's chosen chemotherapy drug (capecitabine, gemcitabine, vinorelbine, docetaxel, albumin-bound paclitaxel, or eribulin) monotherapy
开始日期2023-12-01 |
申办/合作机构 |
恩沃利单抗联合含铂双药化疗对比安慰剂联合含铂双药化疗用于可切除III期非小细胞肺癌患者新辅助/辅助治疗的随机、对照、双盲、多中心III期临床研究
比较恩沃利单抗联合化疗与安慰剂联合化疗新辅助/辅助治疗可手术切除非小细胞肺癌受试者的主要病理学缓解率和无事件生存期。
开始日期2023-11-27 |
申办/合作机构  江苏康宁杰瑞生物制药有限公司 江苏康宁杰瑞生物制药有限公司 [+1] |
100 项与 江苏康宁杰瑞生物制药有限公司 相关的临床结果
登录后查看更多信息
0 项与 江苏康宁杰瑞生物制药有限公司 相关的专利(医药)
登录后查看更多信息
2,444
项与 江苏康宁杰瑞生物制药有限公司 相关的新闻(医药)2024-05-07
·医药笔记
▎Armstrong2024年5月7日,赛诺菲Fitusiran注射液的上市申请获得NMPA受理,这也是Fitusiran的全球首报,有望实现中国率先上市。Fitusiran为一款靶向抗凝血酶(AT)的siRNA疗法。Fitusiran原本预计2022年递交上市申请,后因为安全性问题进行剂量调整,注册时间表也相应地有了延迟。在A型或B型血友病中,凝血因子FVIII或FIX凝血酶的缺失导致凝血酶产生不足,造成出血,传统的治疗方式为凝血因子替代治疗。最新的治疗方案还有FIX/FX双抗、凝血因子AAV基因疗法等。Fitusiran则通过干扰抗凝血酶的表达,提高血液中凝血酶的含量。Fitusiran的临床推进过程如下图所示。通过临床探索,最终将Fitusiran治疗的目标为抗凝血酶范围确定为15-35%,并由此确定剂量调整方案。总结赛诺菲于2018年收购血友病龙头企业Bioverativ,此后又推出迭代每周给药一次的超长效重组凝血八因子BIVV001。Fitusiran只需要每个月给药一次,且对A型或B型血友病都有效,期待其早日上市,造福血友病患者。Armstrong技术全梳理系列GPRC5D靶点全梳理;CD40靶点全梳理;CD47靶点全梳理;补体靶向药物技术全梳理;补体药物:眼科治疗的重要方向;Claudin 6靶点全梳理;Claudin 18.2靶点全梳理;靶点冷暖,行业自知;中国大分子新药研发格局;被炮轰的“me too”;佐剂百年史;胰岛素百年传奇;CUSBEA:风雨四十载;中国新药研发的焦虑;中国生物医药企业的研发竞争;中国双抗竞争格局;中国ADC竞争格局;中国双抗技术全梳理;中国ADC技术全梳理;Ambrx技术全梳理;Vir Biotech技术全梳理;Immune-Onc技术全梳理;亘喜生物技术全梳理;康哲药业技术全梳理;科济药业技术全梳理;恺佧生物技术全梳理;同宜医药技术全梳理;百奥赛图技术全梳理;腾盛博药技术全梳理;创胜集团技术全梳理;永泰生物技术全梳理;中国抗体技术全梳理;德琪医药技术全梳理;德琪医药技术全梳理2.0;和铂医药技术全梳理;荣昌生物技术全梳理;再鼎医药技术全梳理;药明生物技术全梳理;恒瑞医药技术全梳理;豪森药业技术全梳理;正大天晴技术全梳理;吉凯基因技术全梳理;基石药业技术全梳理;百济神州技术全梳理;百济神州技术全梳理第2版;信达生物技术全梳理;信达生物技术全梳理第2版;中山康方技术全梳理;复宏汉霖技术全梳理;先声药业技术全梳理;君实生物技术全梳理;嘉和生物技术全梳理;志道生物技术全梳理;道尔生物技术全梳理;尚健生物技术全梳理;康宁杰瑞技术全梳理;科望医药技术全梳理;科望医药技术全梳理2.0;岸迈生物技术全梳理;礼进生物技术全梳理;康桥资本技术全梳理;余国良的抗体药布局;荃信生物技术全梳理;安源医药技术全梳理;三生国健技术全梳理;仁会生物技术全梳理;乐普生物技术全梳理;同润生物技术全梳理;宜明昂科技术全梳理;派格生物技术全梳理;迈威生物技术全梳理;Momenta技术全梳理;NGM技术全梳理;普米斯生物技术全梳理;普米斯生物技术全梳理2.0;三叶草生物技术全梳理;贝达药业抗体药全梳理;泽璟制药抗体药全梳理;恒瑞医药抗体药全梳理;齐鲁制药抗体药全梳理;石药集团抗体药全梳理;豪森药业抗体药全梳理;华海药业抗体药全梳理;科伦药业抗体药全梳理;百奥泰技术全梳理;凡恩世技术全梳理。
siRNA基因疗法
2024-05-07
以往最显耀的成功经验,在产业发展新格局中不再适用,而经营惯性让其在一次次产业的变革中,未踏准节奏,错失了先机。撰文| 润屿编辑| 顿河 Erin步长制药的棋,到了最难下的时候。5月7日,步长制药发布公告,称全资子公司陕西步长制药有限公司对其产品脑心通胶囊挂网价格进行了下调,目前已挂网省份均已执行调整后价格。具体来看,原规格36粒/盒原价为21.89元-23.69元,调整后为19.90元;48粒/盒原价为28.95元-31.59元,调整后为26.26元;72粒/盒原价为48.31元,调整后为38.81元。平均每粒降价在5分到1.3角之间。脑心通胶囊是步长制药心脑血管用药领域三大独家中药品种之一(其余两款为稳心颗粒和丹红注射液),心脑血管领域又是步长制药的营收大头,收入远高于妇科、泌尿、医疗器械板块。2023年,脑心通胶囊合计销售额为29.37亿元,占同期主营业务收入比例为22.2%;2024年第一季度销售额为5.77亿元,占比达21.87%。步长制药在公告里表示,此次价格调整是根据国家医保局相关文件精神进行的调整,可能对脑心通胶囊销售业绩造成一定影响。近年来,脑心通经历了三个关键性事件:2020年,国家药监局要求对脑心通(片剂、胶囊剂、丸剂)说明书中“不良反应”“禁忌”和“注意事项”项进行修订。被国家药监局“点名”一事,使该产品临床使用受限。2021年,首个公开围绕中成药的集采联盟——广东区域联盟启动中成药集采,多个基本医保药品目录内的中药大品种悉数在列,但步长药业脑心通胶囊最终未中标,是未中标产品中按最高日服用价格估算市场规模最大的产品。而躲过了昔日集采的脑心通,在2024年进一步升级的药价治理中却遭遇了“约谈”降价。4月,山西省药械集中竞价采购网发布《关于部分企业相关产品调价的通知》,称据国家医保局《关于通报部分价格虚高药品约谈结果并抓好落实的函》相关要求,将部分产品价格进行调整,其中有辉瑞阿托伐他汀钙片(立普妥)及苯磺酸氨氯地平片(络活喜),还有步长制药的脑心通胶囊,其价格调整信息与此次公告一致。降价、撤网、甚至是被纳入企业信用评级、取消挂网资格等事件的发生,象征着一个更严、更细、更缜密的集采常态化阶段到来。而在此影响下,那些涉事药企的盈利空间有可能被大大压缩,其未来甚至会被大大地打上问号。步长制药是其中的代表性企业之一。此次大单品脑心通胶囊被“约谈”降价,基于一大非常不乐观的语境:步长制药近两年业绩表现不佳,手握的另几张“王牌”,也不太打得动。2021年-2023年,步长制药营收持续出现负增长,且一年比一年更甚,2023年,公司营收为132.45亿元,在近10年来首度出现两位数的降幅。其中,脑心通胶囊销售量较上一年有所减少。尤其是36粒/盒规格,销量同比下降24.98%,库存量增加113.6%。另一关键品种稳心颗粒的生产量、销售量、库存量相比上年降幅也较大。今年第一季度,步长制药营收与净利双双承压:营收为26.41亿元,同比下降24.88%,净利润达1.14亿元,同比大降74.96%。在中成药企业业绩于寒冬中逆势回暖的大趋势下,步长制药这样的净利表现,显得尤为醒目。产品之外,步长制药在今年备受产业界关注的还有两个“高”:存货过高及商誉过高。步长制药曾是加速并购重组中的一员,分别于2013年-2015年三年时间内累计收购了通化谷红100%的股权,又分别于2012年、2015年累计收购吉林天成95%股权。两桩收购,使步长制药获得了通化谷红的核心产品谷红注射液,以及吉林天成的独家品种复方曲肽注射液和复方脑肽节苷脂注射液。完成两家公司收购后,确认的商誉金额为49.97亿元。2018年以来,步长制药还陷入频繁的资本运作和高溢价收购的争议当中。财报显示,截至2023年底,步长制药商誉账面价值仍高达14.73亿元。此外,同期步长制药存货高达49.3亿元,较上期同比增长30%。颇有点“雪上加霜”意味的是,从通化谷红和吉林天成收购得来的关键产品,自2020年起,陆续被调出了各省的医保目录,截至2022年末全部退出。其中有一段时间,复方曲肽注射液甚至还被吉林省药监局责令暂停了生产销售。核心产品销售疲软,药价治理进一步露“威严”,商誉减值风险尚未化解,库存压力又至,步长制药这家曾经的中药龙头企业,遇到了传统药企在政策推动下的产业剧烈结构性调整时,都会遇到的局面:以往最显耀的成功经验,在产业发展新格局中不再适用,而经营惯性让其在一次次产业的变革中,未踏准节奏,错失了先机。精彩推荐CM10 | 集采 | 国谈 | 医保动态 | 药审 | 人才 | 薪资 | 榜单 | CAR-T | PD-1 | mRNA | 单抗 | 商业化 | 国际化 | 猎药人系列专题 | 出海启思会 | 声音·责任 | 创百汇 | E药经理人理事会 | 微解药直播 | 大国新药 | 营销硬观点 | 投资人去哪儿 | 分析师看赛道 | 药事每周谈 | 医药界·E药经理人 | 中国医药手册创新100强榜单 | 恒瑞 | 中国生物制药 | 百济 | 石药 | 信达 | 君实 | 复宏汉霖 |翰森 | 康方生物 | 上海医药 | 和黄医药 | 东阳光药 | 荣昌 | 亚盛医药 | 齐鲁制药 | 康宁杰瑞 | 贝达药业 | 微芯生物 | 复星医药 |再鼎医药|亚虹医药跨国药企50强榜单 | 辉瑞 | 艾伯维 | 诺华 | 强生 | 罗氏 | BMS | 默克 | 赛诺菲 | AZ | GSK | 武田 | 吉利德科学 | 礼来 | 安进 | 诺和诺德 | 拜耳 | 莫德纳 | BI | 晖致 | 再生元
带量采购一致性评价
2024-05-07
5 月 6 日,BMS 宣布 O 药皮下注射制剂生物制品许可申请(BLA)获 FDA 受理,用于 Opdivo 此前批准上市的所有实体瘤适应症,包括单药治疗、联合伊匹木单抗治疗后的单药维持治疗、与化疗或者卡博替尼联合使用。PDUFA 日期为 2025 年 2 月 28 日。来自:BMS 官网O 药皮下注射制剂由纳武利尤单抗与 Halozyme 专有的重组人透明质酸酶 PH20(rHuPH20)组成。此次上市申请主要基于 III 期临床 CheckMate-67T 研究数据,该研究旨在评估 O 药皮下注射对比静脉输注在既往接受过全身治疗的晚期或转移性透明细胞肾细胞癌(ccRCC)患者中的疗效。研究共纳入 495 名受试者,结果显示,与静脉输注相比,皮下注射剂型在 28 天的时间段内平均血清浓度(Cavgd28)和稳态血清低谷浓度(Cminss)指标上表现出非劣效性,达到共同主要终点。在关键次要终点上,皮下注射与静脉注射 O 药在 ORR 方面表现相似,皮下注射组患者 ORR 为 24.2%,而静脉输注组患者的 ORR 为 18.2%。且在安全性方面,皮下注射与静脉输注两者无明显差异。CheckMate-67T 研究结果来自:Insight 数据库网页版相较于静脉注射剂型,皮下注射制剂独具依从性优势,给药快、便捷性高,可将给药时间大幅缩短,从数小时直接压到以分钟计。各大 MNC 最早自 2015 年开始就已经投入 PD-(L)1 皮下注射剂的研发,尤其是本身拥有同靶点已上市产品的企业。布局企业除 BMS 外,还包括默沙东、罗氏等。全球范围内首个获批上市的 PD-L1 单抗皮下制剂是康宁杰瑞/思路迪/先声药业的恩沃利单抗。不过从海外市场来看,罗氏阿替利珠单抗(SC)于去年 8 月在英国批准上市,今年 1 月获欧盟批准;而在美国,由于生产工艺的更新需求,上市时间将推迟至今年。而此次 O 药的申报上市,有望成为首个获批上市的 PD-1 单抗皮下制剂。默沙东 K 药皮下注射制剂已处于 III 期临床阶段,III 期 MK-3475-A86 试验旨在评估皮下给药与化疗联用,对比静脉给药与化疗联用,一线治疗鳞状和非鳞状 NSCLC,已于上个月完成试验主要指标。同时,默沙东还布局了 K 药+透明质酸酶复方制剂皮下注射剂 MK-3475A,正在开展一线治疗 NSCLC 的 III 期 MK-3475A-D77 临床试验,预计于今年 9 月完成主要指标。辉瑞布局的 Sasanlimab 则针对非肌层浸润性膀胱癌正在开展 III 期,预计今年 6 月完成主要指标。国产企业中,百济、恒瑞、君实等均有布局。进展最快的是君实 JS001sc,是在已上市产品特瑞普利单抗注射液的基础上开发的,刚于上个月月底登记启动了 III 期临床试验,一线治疗非鳞 NSCLC(登记号:CTR20241554),成为国产首个进入 III 期临床的 PD-1 单抗。恒瑞 SHR-1901 属于 PD-1 皮下注射剂。2021 年 8 月,SHR-1901 首次在国内获批临床;正在开展 I 期临床试验。百济替雷利珠单抗皮下注射剂同样在开展 I 期临床,一线治疗 NSCLC(登记号:CTR20233814)。封面来源:站酷海洛 Plus免责声明:本文仅作信息分享,不代表 Insight 立场和观点,也不作治疗方案推荐和介绍。如有需求,请咨询和联系正规医疗机构。编辑:HebePR 稿对接:微信 insightxb投稿:微信 insightxb;邮箱 insight@dxy.cn多样化功能、可溯源数据……Insight 数据库网页版等你体验点击阅读原文,立刻解锁!
临床3期上市批准
100 项与 江苏康宁杰瑞生物制药有限公司 相关的药物交易
登录后查看更多信息
100 项与 江苏康宁杰瑞生物制药有限公司 相关的转化医学
登录后查看更多信息
管线布局
2024年05月17日管线快照
管线布局中药物为当前组织机构及其子机构作为药物机构进行统计,早期临床1期并入临床1期,临床1/2期并入临床2期,临床2/3期并入临床3期
临床前
11
1
临床1期
临床2期
2
3
临床3期
批准上市
1
12
其他
登录后查看更多信息
当前项目
| 药物(靶点) | 适应症 | 全球最高研发状态 |
|---|---|---|
贝拉西普生物类似药 (苏州康宁杰瑞) ( CD80 x CD86 ) | 类风湿关节炎 更多 | 临床2期 |
恩沃利单抗 ( PDL1 ) | 肝细胞癌 更多 | 临床1/2期 |
JSKN-003 ( HER2 x TOP1 ) | 晚期恶性实体瘤 更多 | 临床1/2期 |
JSKN-033 ( HER2 x PDL1 ) | 实体瘤 更多 | 临床1/2期 |
重组人源化抗HER2双特异性抗体(康宁杰瑞) ( HER2 ) | 乳腺癌 更多 | 临床1期 |
登录后查看更多信息
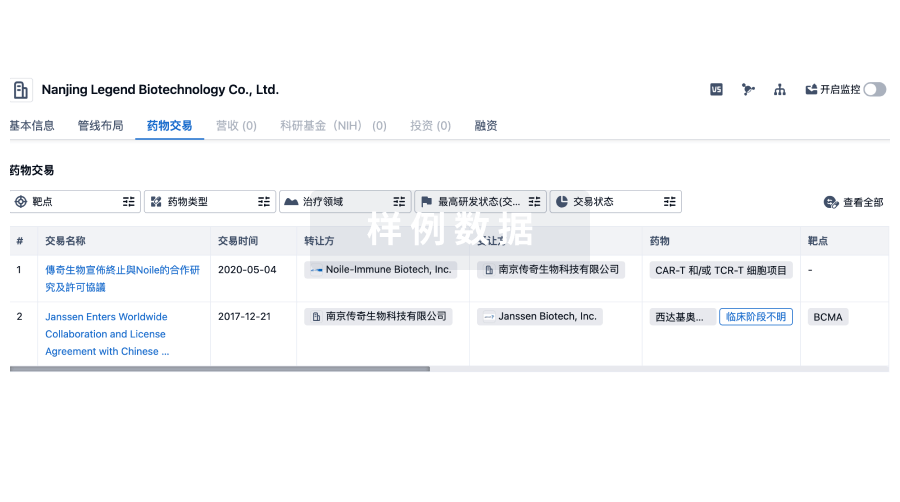
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
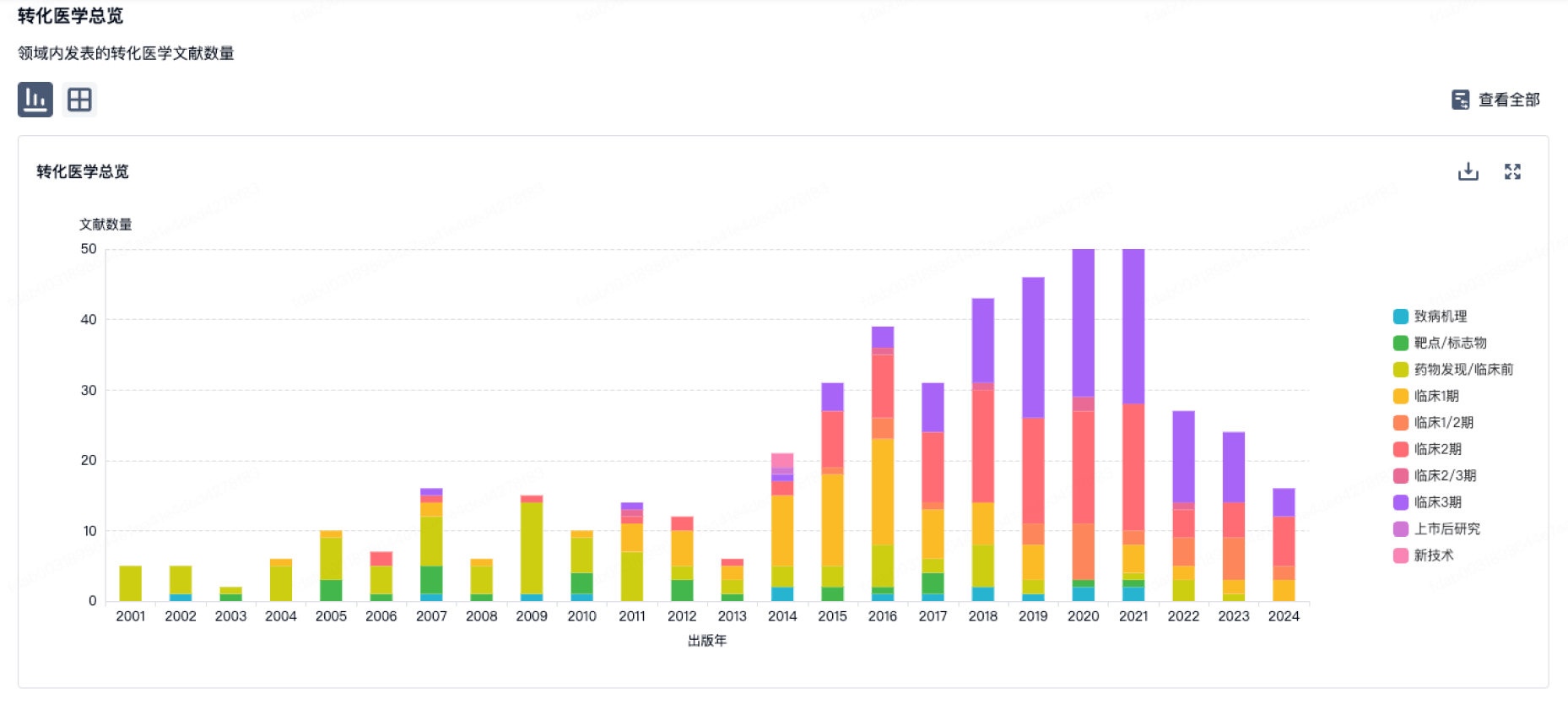
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
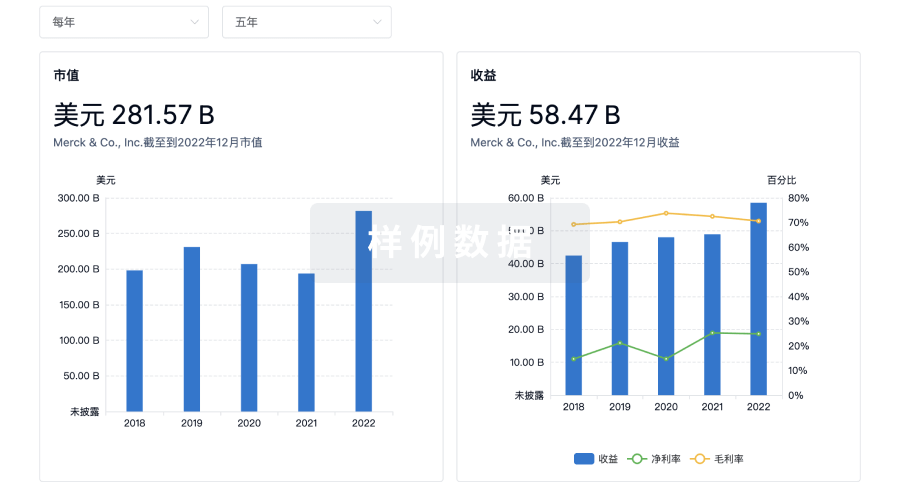
营收
使用 Synapse 探索超过 36 万个组织的财务状况。
登录
或
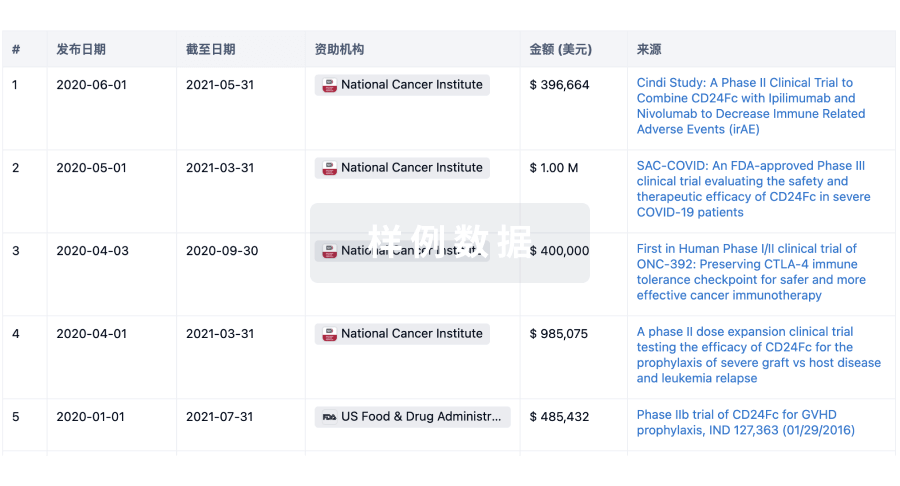
科研基金(NIH)
访问超过 200 万项资助和基金信息,以提升您的研究之旅。
登录
或
投资
深入了解从初创企业到成熟企业的最新公司投资动态。
登录
或
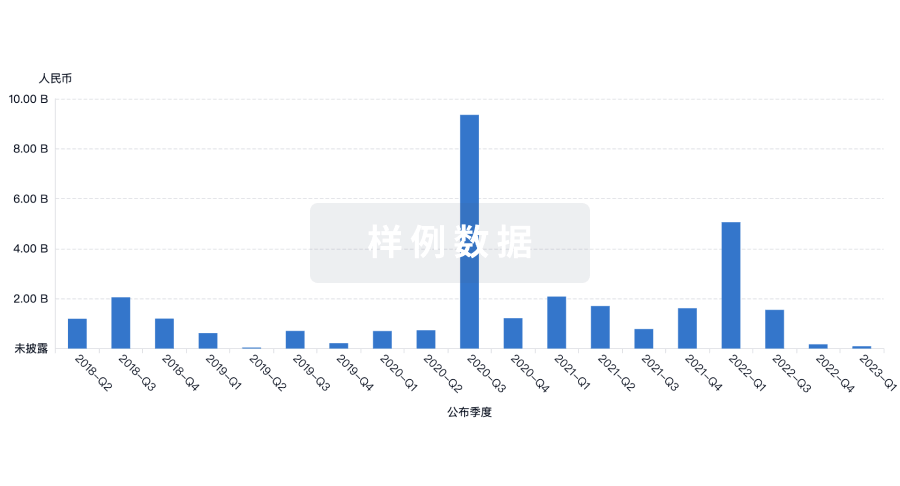
融资
发掘融资趋势以验证和推进您的投资机会。
登录
或
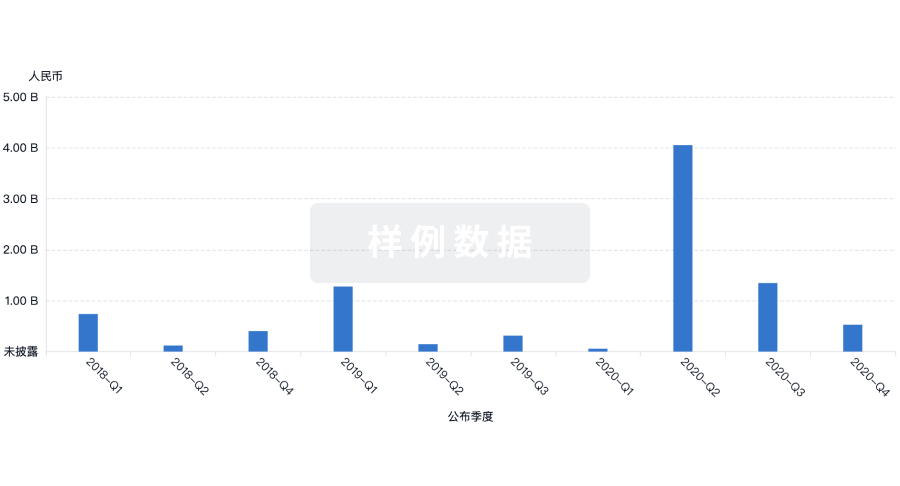
标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用


