更新于:2024-05-01

Lepu Biopharma Co., Ltd.
更新于:2024-05-01
概览
标签
肿瘤
消化系统疾病
呼吸系统疾病
ADC
单克隆抗体
溶瘤病毒
疾病领域得分
一眼洞穿机构专注的疾病领域
暂无数据
技术平台
公司药物应用最多的技术
暂无数据
靶点
公司最常开发的靶点
暂无数据
| 排名前五的药物类型 | 数量 |
|---|---|
| ADC | 6 |
| 单克隆抗体 | 2 |
| 双特异性抗体 | 1 |
| 溶瘤病毒 | 1 |
关联
18
项与 乐普生物科技股份有限公司 相关的药物靶点 |
作用机制 PD-1抑制剂 |
在研机构 |
原研机构 |
最高研发阶段批准上市 |
首次获批国家/地区 中国 |
首次获批日期2022-07-19 |
作用机制 CLDN18.2抑制剂 [+1] |
在研机构 |
非在研适应症- |
最高研发阶段临床3期 |
首次获批国家/地区- |
首次获批日期- |
靶点 |
作用机制 CSF-2R刺激剂 |
在研适应症 |
最高研发阶段临床3期 |
首次获批国家/地区- |
首次获批日期- |
77
项与 乐普生物科技股份有限公司 相关的临床试验在卡介苗(BCG)无应答的非肌层浸润性膀胱癌患者中评价CG0070注射液局部多次给药的耐受性、安全性和初步疗效的单臂、开放、多中心、剂量递增Ⅰ期临床研究
评价溶瘤腺病毒CG0070多次给药(膀胱灌注)治疗BCG无应答的非肌层浸润性膀胱癌患者的安全性、耐受性,明确剂量限制性毒性(DLT)。
进一步确定CG0070多次给药最大耐受剂量(MTD)及推荐的II期临床剂量(RP2D)。
开始日期2023-11-14 |
申办/合作机构  乐普生物科技股份有限公司 乐普生物科技股份有限公司 [+2] |
An Open-label, Randomized, Multi-center, Phase III Clinical Study of MRG002 Versus Investigator's Choice of Chemotherapy in the Treatment of Patients With HER2-positive Unresectable Locally Advanced or Metastatic Urothelial Cancer Previously Treated With Platinum-based Chemotherapy and PD-1/PD-L1 Inhibitors
The primary objective of this study is to compare the overall survival (OS) and progression-free survival (PFS) between MRG002 and investigator selected chemotherapy in patients with HER2-positive unresectable locally advanced or metastatic urothelial cancer previously treated with platinum-based chemotherapy and PD-1/PD-L1 inhibitors.
开始日期2023-04-06 |
申办/合作机构 |
MRG003对比西妥昔单抗/甲氨蝶呤在二/三线治疗复发或转移性头颈鳞癌患者的随机、开放、多中心III期研究
本研究是一项随机、开放、多中心III期研究,在既往接受过PD-1(L1)抑制剂和铂类药物治疗失败的复发或转移性头颈鳞癌患者中,比较MRG003与西妥昔单抗/甲氨蝶呤在二/三线治疗复发或转移性头颈鳞癌患者中的疗效和安全性。
开始日期2023-03-29 |
申办/合作机构 |
100 项与 乐普生物科技股份有限公司 相关的临床结果
登录后查看更多信息
0 项与 乐普生物科技股份有限公司 相关的专利(医药)
登录后查看更多信息
1,499
项与 乐普生物科技股份有限公司 相关的新闻(医药)2024-04-07
·医药笔记
▎Armstrong2024年4月7日,北京市医疗保障局发布“关于对《北京市医疗保障局等9部门北京市支持创新医药高质量发展若干措施(2024)(征求意见稿)》公开征求意见的公告”。此次征求意见稿措施详细且具体,公开征集时间仅3个工作日,可见决心之大、效率之高。整个征求意见稿包括八个部分,第一“着力提升创新医药临床研究质效”,第二“助力创新药械审评审批”,第三“大力促进医药贸易便利化”,第四“加力促进创新医药临床应用”,第五“努力拓展创新医药支付渠道”,第六“鼓励医疗健康数据赋能创新”,第七“强化创新医药企业投融资支持”,第八“保障措施”。从临床研究端、审评端、进出口贸易端、支付端、数据端、投融资端全链条支持创新医药行业发展。临床研究第一条明确提出将临床试验启动整体用时压缩至28周内,其他措施包括组建10家以上区域临床研究联合体,鼓励社会资本投资建设研究型医院,扩大医学伦理审查互认范围等。审批端的目标更为具体,IND审批时间从60天压缩至30天,药品补充申请审评时间从200天压缩至60天,对创新药实施项目制管理,提前介入并全程指导等。对于医药贸易,2024年力争推动10个进口品种打通落地,同时推动5个品种出口。对于上市创新药,多渠道推动临床应用,拓展支付渠道。临床应用端,减少DRG等对创新药的应用限制,剔除国谈药、创诊疗项目对人均药品费用、分均医疗费用等指标的影响。支付端方面,鼓励创新药参与医保谈判,鼓励覆盖创新药械的商业保险,建立“北京普惠健康保”特药清单动态调整机制。鼓励医疗健康高价值数据的应用,赋能行业创新。投融资端,用好北京市医药健康产业投资基金,带动社会投资,加强医药企业资本市场全链条服务。最后是保障措施。总结2023年8月,国务院常务会议上审议通过《医药工业高质量发展行动计划(2023-2025年)》,医药行业的政策春风已经呼之欲出。此次北京市率先推出医药行业的全链条政策性扶持政策,从征集意见稿的内容,以及征集意见时间仅3天等可以看到,此次支持政策的决心和力度之大,且可以预见很快各地政府也都会出台类似的措施。从实施举措来看,覆盖了临床开发、审评审批、临床应用与支付、进出口、投融资等,在全链条都给出了具体措施和目标。持续三年的资本市场寒冬之下,医药行业终于迎来全面政策支持,或将拥抱久违的春天。Armstrong技术全梳理系列GPRC5D靶点全梳理;CD40靶点全梳理;CD47靶点全梳理;补体靶向药物技术全梳理;补体药物:眼科治疗的重要方向;Claudin 6靶点全梳理;Claudin 18.2靶点全梳理;靶点冷暖,行业自知;中国大分子新药研发格局;被炮轰的“me too”;佐剂百年史;胰岛素百年传奇;CUSBEA:风雨四十载;中国新药研发的焦虑;中国生物医药企业的研发竞争;中国双抗竞争格局;中国ADC竞争格局;中国双抗技术全梳理;中国ADC技术全梳理;Ambrx技术全梳理;Vir Biotech技术全梳理;Immune-Onc技术全梳理;亘喜生物技术全梳理;康哲药业技术全梳理;科济药业技术全梳理;恺佧生物技术全梳理;同宜医药技术全梳理;百奥赛图技术全梳理;腾盛博药技术全梳理;创胜集团技术全梳理;永泰生物技术全梳理;中国抗体技术全梳理;德琪医药技术全梳理;德琪医药技术全梳理2.0;和铂医药技术全梳理;荣昌生物技术全梳理;再鼎医药技术全梳理;药明生物技术全梳理;恒瑞医药技术全梳理;豪森药业技术全梳理;正大天晴技术全梳理;吉凯基因技术全梳理;基石药业技术全梳理;百济神州技术全梳理;百济神州技术全梳理第2版;信达生物技术全梳理;信达生物技术全梳理第2版;中山康方技术全梳理;复宏汉霖技术全梳理;先声药业技术全梳理;君实生物技术全梳理;嘉和生物技术全梳理;志道生物技术全梳理;道尔生物技术全梳理;尚健生物技术全梳理;康宁杰瑞技术全梳理;科望医药技术全梳理;科望医药技术全梳理2.0;岸迈生物技术全梳理;礼进生物技术全梳理;康桥资本技术全梳理;余国良的抗体药布局;荃信生物技术全梳理;安源医药技术全梳理;三生国健技术全梳理;仁会生物技术全梳理;乐普生物技术全梳理;同润生物技术全梳理;宜明昂科技术全梳理;派格生物技术全梳理;迈威生物技术全梳理;Momenta技术全梳理;NGM技术全梳理;普米斯生物技术全梳理;普米斯生物技术全梳理2.0;三叶草生物技术全梳理;贝达药业抗体药全梳理;泽璟制药抗体药全梳理;恒瑞医药抗体药全梳理;齐鲁制药抗体药全梳理;石药集团抗体药全梳理;豪森药业抗体药全梳理;华海药业抗体药全梳理;科伦药业抗体药全梳理;百奥泰技术全梳理;凡恩世技术全梳理。
临床申请
2024-04-07
·医药笔记
▎Armstrong2024年4月5日,阿斯利康在Clinicaltrials.gov网站上注册了三期临床试验TROPION-Lung14,奥希替尼联合或不联合Trop2 ADC新药Dato-DXd一线治疗EGFR突变阳性非小细胞肺癌。该三期临床计划入组582例晚期EGFR突变阳性非小细胞肺癌患者,预计2028年3月完成。奥希替尼+化疗已经获批一线治疗,Trop2 ADC则已经在二线后治疗EGFR突变NSCLC积累部分数据,此次奥希替尼+Trop2 ADC联合治疗则是进一步的进化。TROPION-Lung01、TROPION-Lung05中,Dato-DXd在后线治疗AGA NSCLC中获得积极数据。总结肺癌为阿斯利康的优势领域,手握奥希替尼、DS-8201、Dato-DXd等多款重磅炸弹,阿斯利康工具箱极为丰富,为联合治疗提供了充分的设计空间。靶向治疗+ADC,可以看做小分子靶向治疗+靶向化疗的升级版。Armstrong技术全梳理系列GPRC5D靶点全梳理;CD40靶点全梳理;CD47靶点全梳理;补体靶向药物技术全梳理;补体药物:眼科治疗的重要方向;Claudin 6靶点全梳理;Claudin 18.2靶点全梳理;靶点冷暖,行业自知;中国大分子新药研发格局;被炮轰的“me too”;佐剂百年史;胰岛素百年传奇;CUSBEA:风雨四十载;中国新药研发的焦虑;中国生物医药企业的研发竞争;中国双抗竞争格局;中国ADC竞争格局;中国双抗技术全梳理;中国ADC技术全梳理;Ambrx技术全梳理;Vir Biotech技术全梳理;Immune-Onc技术全梳理;亘喜生物技术全梳理;康哲药业技术全梳理;科济药业技术全梳理;恺佧生物技术全梳理;同宜医药技术全梳理;百奥赛图技术全梳理;腾盛博药技术全梳理;创胜集团技术全梳理;永泰生物技术全梳理;中国抗体技术全梳理;德琪医药技术全梳理;德琪医药技术全梳理2.0;和铂医药技术全梳理;荣昌生物技术全梳理;再鼎医药技术全梳理;药明生物技术全梳理;恒瑞医药技术全梳理;豪森药业技术全梳理;正大天晴技术全梳理;吉凯基因技术全梳理;基石药业技术全梳理;百济神州技术全梳理;百济神州技术全梳理第2版;信达生物技术全梳理;信达生物技术全梳理第2版;中山康方技术全梳理;复宏汉霖技术全梳理;先声药业技术全梳理;君实生物技术全梳理;嘉和生物技术全梳理;志道生物技术全梳理;道尔生物技术全梳理;尚健生物技术全梳理;康宁杰瑞技术全梳理;科望医药技术全梳理;科望医药技术全梳理2.0;岸迈生物技术全梳理;礼进生物技术全梳理;康桥资本技术全梳理;余国良的抗体药布局;荃信生物技术全梳理;安源医药技术全梳理;三生国健技术全梳理;仁会生物技术全梳理;乐普生物技术全梳理;同润生物技术全梳理;宜明昂科技术全梳理;派格生物技术全梳理;迈威生物技术全梳理;Momenta技术全梳理;NGM技术全梳理;普米斯生物技术全梳理;普米斯生物技术全梳理2.0;三叶草生物技术全梳理;贝达药业抗体药全梳理;泽璟制药抗体药全梳理;恒瑞医药抗体药全梳理;齐鲁制药抗体药全梳理;石药集团抗体药全梳理;豪森药业抗体药全梳理;华海药业抗体药全梳理;科伦药业抗体药全梳理;百奥泰技术全梳理;凡恩世技术全梳理。
抗体药物偶联物临床3期申请上市医药出海引进/卖出
2024-04-07
·药智网
春暖花开的季节,也是各家年报密集披露的时期,有人欢喜有人愁。其中,有这样一家Biotech企业,收入同比增加1347.2%,年内亏损大幅减少96.8%,盈利在望。这就是乐普生物。作为一家“小而美”的ADC Biotech,乐普生物如何突出重围?01“小而精”研发路线不同于某些Biotech追求“大而全”(囊括各种药物类型、堆砌管线),乐普生物主要走“小而精”研发路线,即聚焦于具有差异化竞争优势的ADC药物研发。众所周知,当前ADC药物主要扎堆热门靶点HER2,后来者想在激烈的市场竞争中占得一席之地,难度非常大。而选择布局差异化靶点,或避开热门癌种,是明智的策略。基于此,乐普生物布局了具备差异化优势的ADC管线,包括MRG003(EGFR靶向ADC)、MRG002(HER2靶向ADC)、MRG004A(TF靶向ADC)、MRG001(CD20靶向ADC)、CMG901(CLDNI8.2靶向ADC),其中有些ADC具备BIC或FIC潜力。乐普生物研发管线图片来源:乐普生物2023年财报例如,MRG003是国内首创的EGFR ADC,适应症主要针对二线及以上NPC(鼻咽癌)、HNSCC(头颈部鳞状细胞癌),目前均已开展III期试验,进度处于全球前三、国内第一,今年还有望申报鼻咽癌适应症上市。鼻咽癌虽不是大癌种,却存在巨大的临床未满足需求,单药化疗或PD-1/PD-L1抑制剂二线及以上治疗复发转移性鼻咽癌的ORR仅20%-30%,疗效有限。相较之下,MRG003在鼻咽癌IIa期研究中展现了亮眼数据:针对经PD-1/PD-L1及含铂化疗治疗的NPC患者,ORR为47.4%。2.0mg/kg剂量组的ORR为39.2%,mPFS为7.3个月;2.3mg/kg剂量组的ORR为55.2%。基于良好的数据,FDA授予MRG003治疗鼻咽癌的孤儿药认定、快速通道资格。临近商业化的ADC药物,还有靶向HER2的MRG002。目前,MRG002正在中国进行HER2高表达乳腺癌肝转移II期关键临床试验,并已观察到良好数据,正在做报产准备。同时,正在开展针对HER2阳性乳腺癌、尿路上皮癌患者的III期临床试验。乐普生物的“小而精”研发路线,不仅反映在适应症的选择,还体现在PD-1+ADC联合疗法的研发上。据华创证券研报披露,现有的IO疗法中,近一半方案可能从IO+化疗升级为IO+ADC,相关适应症市场有望实现100-200%扩容。如今,IO+ADC联合疗法已是兵家必争之地。图片来源:华创证券研报目前,乐普生物“普特利单抗+MRG003”已在鼻咽癌及头颈部鳞状细胞癌II期试验中观察到良好的数据,“普特利单抗+MRG002”正在进行治疗HER2表达实体瘤患者的II期试验,并在尿路上皮癌患者中观察到良好的初步数据。除MRG003外,MRG004A同样瞄准未满足的临床需求,且是国内首个申报临床的TF ADC,目前正在中美两国开展治疗复发性或难治性胰腺癌的Ⅰ期临床试验,并已在TNBC(三阴乳腺癌)、CC(宫颈癌)中观察到良好数据。由于胰腺癌起病隐匿、诊断困难,且治疗手段有限、致死率高(患者总生存期仅6-9个月),被医学界称为“癌中之王”。无论PD-1/PD-L1单抗还是ADC“药王”DS-8201,都对胰腺癌束手无策。如果之后MRG004A能拿下胰腺癌,势必成为“香饽饽”。从市场角度看,全球仅有一款TF ADC药物获批上市,来自Seagen的Tivdak,已获批宫颈癌、卵巢癌适应症,再鼎医药拥有中国权益。02减少亏损的秘密随着国内创新药行业遭遇资本“寒冬”,Biotech们使出浑身解数优化现金流管理。乐普生物也不例外,通过综合性收入在2023年度实现亏损大幅收窄,主要得益于商业化收入大幅增加及公司投资活动确认的其他利得增加。其中,PD-1单抗普特利单抗实现销售收入1.01亿元,同比大幅增加551%,与康诺亚合作研发的CLDNI8.2 ADC药物CMG901获得BD及技术服务收入1.24亿元,通过出售皓阳生物15%股权获得收益1.04亿元,持有的武汉滨会因股权摊簿录得收益1.16亿元。乐普生物2023年业绩表现图片来源:乐普生物2023年财报此外,乐普生物还积极采取降本增效措施,提升整体盈利能力。其中,2023年研发开支较2022年5.24亿元减少12.6%,行政开支较2022年1.39亿元减少0.34亿元。面对创新药资本寒冬,Biotech不仅要“节流”,更要“开源”。通过持续进行研发活动,乐普生物已将多款核心管线推至后期研发阶段,同时提前布局ADC联合PD-1适应症市场,实现PD-1销售收入稳步增长,并积极推进海外BD、受托提供CDMO服务。这一时期通常需要大量的资金投入来支持临床试验、生产准备和市场推广等活动。截至2023年,乐普生物现金及现金等价物为4.26亿元,较2022年6.69亿元减少了2.43亿元。不过,在海外BD方面,乐普生物有着明确的战略规划,已储备多款BD资源。这也是未来几年能否实现扭亏为盈的重要看点。03如何冲击盈利?在亏损显著减少后,实现盈利成为乐普生物接下来的目标。这也是所有Biotech的目标。2023年度,有不少Biotech实现扭亏为盈,包括和铂医药、康方生物、和黄医药、复宏汉霖。业绩扭亏的原因,都与对外授权交易有关。实际上,通过对外授权获得现金流、做起CXO(医药外包服务)生意,正是乐普生物实现扭亏为盈的战略要点。2023年,乐普生物将与康诺亚合作研发的潜在首创Claudin 18.2 ADC药物CMG901的全球权益授予跨国制药巨头阿斯利康。目前,乐普生物和康诺亚已获得6300万美元的预付款,未来还将获得高达11亿美元的潜在里程碑付款及高达低双位数的分层特许权使用费。另外,乐普生物还受托提供CDMO服务。去年11月,乐普生物与乐普医疗有条件订立GLP-1等相关产品CDMO服务框架协议,将向乐普医疗及/或其附属公司提供的CDMO服务涵盖CMC技术服务。正如乐普生物在公告中所言,之所以订立CDMO服务框架协议,是考虑到“在适当的机会出现时通过提供CDMO服务更有效利用富余产能,可为公司整体产生补充现金流量”。除CMG901外,乐普生物MRG003、MRG004A都存在BD的机会。MRG003是进度处全球前三的EGFR ADC,正在冲刺商业化,上市后有望享受到市场独占的红利,而且在鼻咽癌、头颈部鳞状细胞癌研究中已观察到令人鼓舞的数据。事实上,基于大药潜质,EGFR靶向药物已成为巨头必争之地,例如EGFR-TKIs类药物“王者”奥希替尼2023年销售额近58亿美元、强生EGFR/c-Met双抗埃万妥单抗剑指50亿美元、百利天恒EGFR/HER3双抗ADC药物BL-B01D1达成最高84亿美元授权交易。MRG004A同样具备大药潜质,全球首款且目前唯一获批的TF ADC产品Tivdak,已验证TF靶点的成药性,机构预测其销售峰值有望超过12亿美元。相较Tivdak,MRG004A已初步显示出一定优势,包括半衰期更长、有效性可能更好,毒性可能更低,安全性较好。为了实现盈利,乐普生物不仅破拆BD的砖墙,还前瞻性布局了溶瘤病毒管线。CG0070便是乐普生物从CG Oncology公司引进的潜在FIC溶瘤病毒疗法,后者已推至临床Ⅲ期阶段,并已展现出比现有获批疗法更优的疗效数据和安全性。目前,乐普生物正在中国开展CG0070的I期临床试验,后续有望开展桥接试验,快速实现上市。更值一提的是,CG0070联合PD-1单抗“全球药王”K药已初步显示出较单药更优异的数据。乐普生物也开展了自身核心产品普特利单抗联用CG0070治疗高危BCG无反应非肌层浸润性膀胱癌的I/II临床。04结语作为一家“小而美”的ADC Biotech,乐普生物选择走“小而精”的研发路线,管线布局可谓一环套一环:以PD-1单抗为基石,顺势开展多项“PD-1单抗+ADC”、“PD-1单抗+溶瘤病毒”联合疗法临床试验。另外,为了能持续开展研发活动、冲击盈利,乐普生物还通过各种渠道或途径获得收入,“精细调配现金流”的策略展露无疑。在创新药投融资遇冷的当下,乐普生物的战略规划无疑起到很好的示范作用。但这也只是起点,在研管线能否实现商业化、何时实现盈利,还有待继续观察。参考资料:1.乐普生物财报、公告、官网2.《大幅缩亏,ADC龙头腾飞在即》,瞪羚社,2024-03-293.华创证券研报声明:本内容仅用作医药行业信息传播,为作者独立观点,不代表药智网立场。如需转载,请务必注明文章作者和来源。对本文有异议或投诉,请联系maxuelian@yaozh.com。责任编辑 | 金银花转载开白 | 马老师 18996384680(同微信)商务合作 | 王存星 19922864877(同微信) 阅读原文,是昨天最受欢迎的文章哦
抗体药物偶联物财报快速通道孤儿药临床3期
100 项与 乐普生物科技股份有限公司 相关的药物交易
登录后查看更多信息
100 项与 乐普生物科技股份有限公司 相关的转化医学
登录后查看更多信息
管线布局
2024年05月17日管线快照
管线布局中药物为当前组织机构及其子机构作为药物机构进行统计,早期临床1期并入临床1期,临床1/2期并入临床2期,临床2/3期并入临床3期
药物发现
1
1
临床申请
临床申请批准
2
1
临床1期
临床2期
4
2
临床3期
批准上市
1
6
其他
登录后查看更多信息
当前项目
| 药物(靶点) | 适应症 | 全球最高研发状态 |
|---|---|---|
普特利单抗 ( PD-1 ) | 黑色素瘤 更多 | 批准上市 |
MRG-002 ( HER2 ) | HER2阳性尿路上皮癌 更多 | 临床3期 |
MRG-003 ( EGFR ) | 鼻咽癌 更多 | 临床3期 |
重组人源化抗PD-L1单克隆抗体(Taizhou HoudeAoke Biomedical Co., Ltd.) ( PDL1 ) | 广泛期小细胞肺癌 更多 | 临床2期 |
MRG-001 ( CD20 x Tubulin ) | 新型冠状病毒感染 更多 | 临床2期 |
登录后查看更多信息
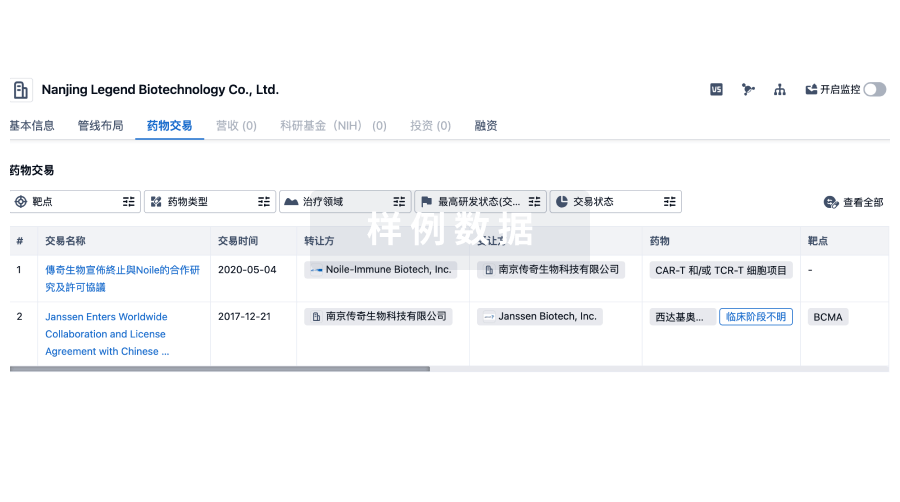
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
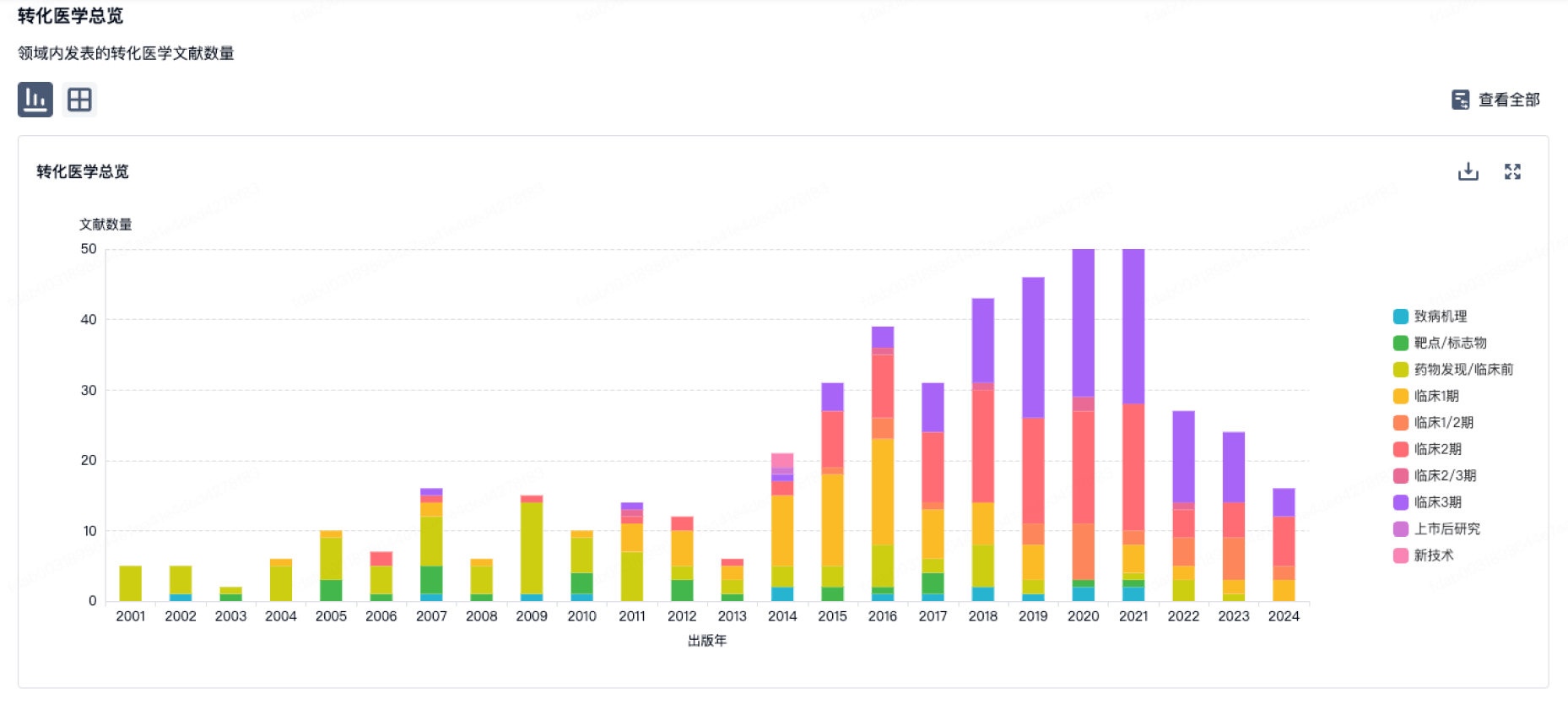
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
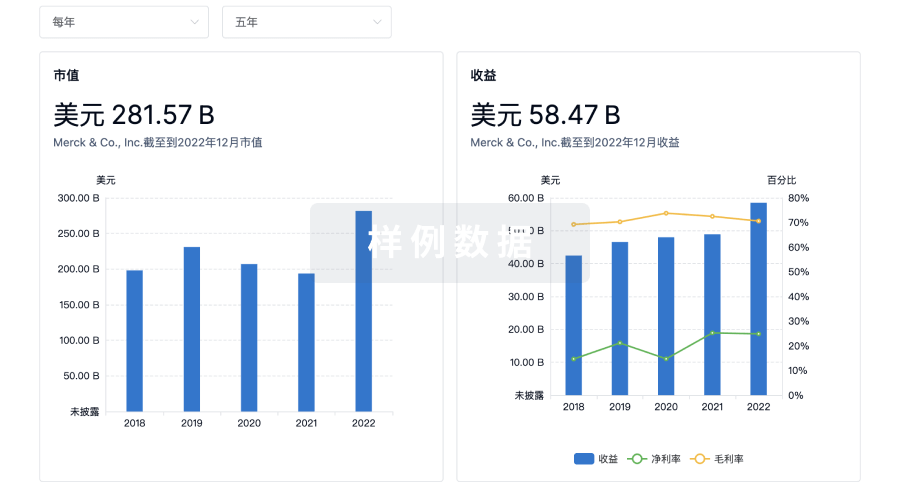
营收
使用 Synapse 探索超过 36 万个组织的财务状况。
登录
或
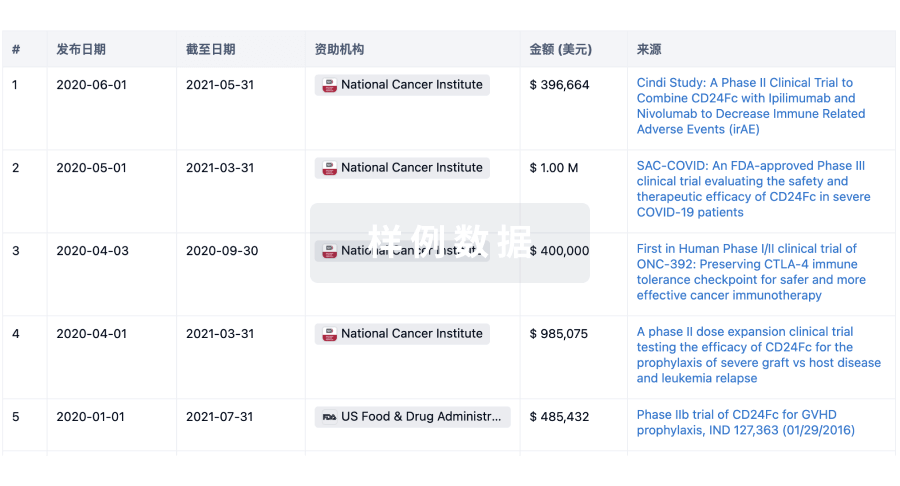
科研基金(NIH)
访问超过 200 万项资助和基金信息,以提升您的研究之旅。
登录
或
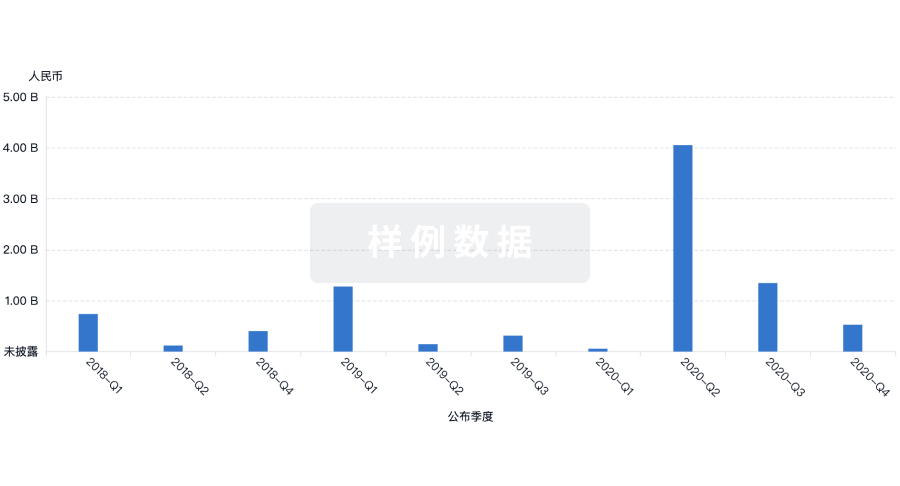
投资
深入了解从初创企业到成熟企业的最新公司投资动态。
登录
或
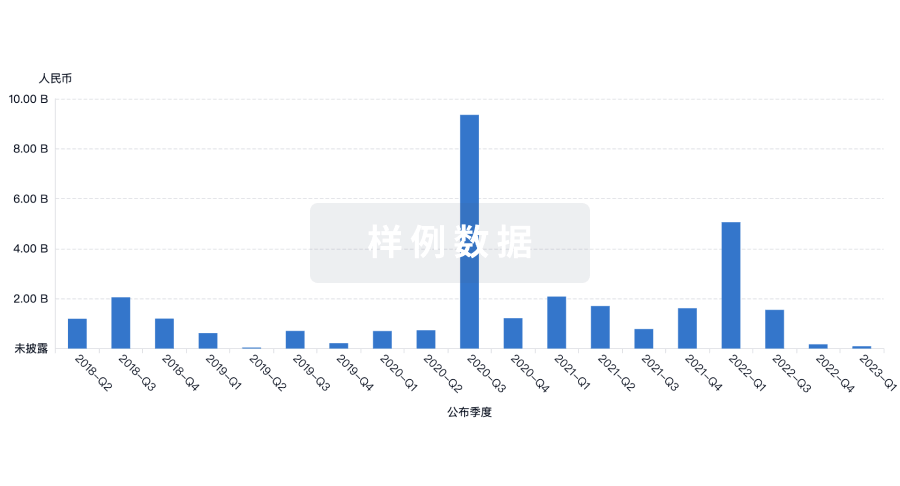
融资
发掘融资趋势以验证和推进您的投资机会。
登录
或
标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用

