更新于:2024-05-16
BPI-16350
更新于:2024-05-16
概要
基本信息
药物类型 小分子化药 |
别名 康美纳、酒石酸泰贝西利 |
作用机制 CDK4抑制剂(细胞周期蛋白依赖性激酶4抑制剂)、CDK6抑制剂(细胞周期蛋白依赖性激酶6抑制剂) |
非在研适应症- |
原研机构 |
在研机构 |
非在研机构- |
最高研发阶段临床3期 |
首次获批日期- |
最高研发阶段(中国)临床3期 |
特殊审评特殊审批 (中国) |
关联
8
项与 BPI-16350 相关的临床试验一项在健康受试者中评价利福平或伊曲康唑对BPI-16350胶囊药代动力学影响的单中心、开放、固定顺序临床试验
本研究旨在确定利福平或伊曲康唑对BPI-16350的暴露量变化是否具有临床显著性,并为临床合并用药提供参考。
开始日期2023-10-24 |
申办/合作机构 |
[14C]BPI-16350在中国男性健康受试者体内的物质平衡临床试验
考察中国男性健康受试者单剂量口服[14C]BPI-16350后体内吸收、代谢和排泄,为药物临床的合理使用提供参考
开始日期2023-06-19 |
申办/合作机构 |
BPI-16350联合氟维司群对比安慰剂联合氟维司群治疗既往接受内分泌治疗后进展的HR+、HER2-的局部晚期、复发或转移性乳腺癌受试者的多中心、随机、双盲、安慰剂对照的Ⅲ期临床研究
主要目的:
评估在既往接受内分泌治疗后进展的HR+/HER2-的晚期乳腺癌受试者中,与安慰剂联合氟维司群相比,BPI-16350胶囊联合氟维司群治疗的有效性。
次要目的:
1)评估BPI-16350胶囊联合氟维司群对比安慰剂联合氟维司群在接受内分泌治疗后进展的HR+/HER2-的晚期乳腺癌受试者中的安全性;
2)评估药物的群体药代动力学特性,并探索药物暴露与疗效、安全性的关系;
3)评估BPI-16350胶囊联合氟维司群对比安慰剂联合氟维司群对受试者健康相关生活质量的影响。
开始日期2022-05-25 |
申办/合作机构 |
100 项与 BPI-16350 相关的临床结果
登录后查看更多信息
100 项与 BPI-16350 相关的转化医学
登录后查看更多信息
100 项与 BPI-16350 相关的专利(医药)
登录后查看更多信息
25
项与 BPI-16350 相关的新闻(医药)2024-05-12
点击蓝字关注我们本周,热点很多。首先是审评审批方面,有几个点值得重点说。比如,正大天晴PD-L1单抗贝莫苏拜单抗获批上市以及再鼎医药引进的创新药瑞普替尼胶囊获批上市;其次是研发方面,信达玛仕度肽首个降糖Ⅲ期研究获积极结果,头对头度拉糖肽;再次是交易及投融资方面,有不少交易,可以一说的是,先为达GLP-1激动剂许可韩国权益,总交易额5600万美元;最后是上市方面,华芢生物港交所递交IPO申请。本周盘点包括审评审批、研发、交易及投融资和上市四大板块,统计时间为5.6-5.11,包含29条信息。 审评审批NMPA上市批准1、5月9日,NMPA官网显示,中国生物制药下属公司正大天晴的贝莫苏拜单抗(benmelstobart,TQB2450)获批上市,用于联合安罗替尼、卡铂和依托泊苷一线治疗广泛期小细胞肺癌(ES-SCLC)患者。TQB2450是正大天晴自主研发的一款靶向PD-L1的新型全人源化IgG1抗体。2、5月9日,NMPA官网显示,卫材的吡仑帕奈片(perampanel)获批新适应症,治疗癫痫全身强直-阵挛发作。吡仑帕奈是一种高选择性、非竞争性AMPA受体拮抗剂,通过与突触后膜上的AMPA受体非竞争性结合从而抑制谷氨酸诱导的神经元过度兴奋,发挥抗癫痫作用。2012年7月,吡仑帕奈首次在欧盟获批上市。3、5月9日,NMPA官网显示,辉凌医药(Ferring)的重组人促卵泡激素δ注射液获批上市,适用于接受辅助生殖技术(如体外受精或胞浆内单精子注射)的女性,用于行控制性卵巢刺激,以诱导多卵泡发育。这是一款从人类细胞系中提取的重组促卵泡激素(rFSH)follitropin delta(商品名:Rekovelle)。4、5月11日,NMPA显示,BMS、再鼎医药的瑞普替尼胶囊(奥凯乐/Augtyro)获批上市,适用于ROS1阳性的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者。瑞普替尼是一种酪氨酸蛋白激酶原癌基因ROS1和原肌球蛋白受体酪氨酸激酶(TRKs)TRKA、TRKB及TRKC的抑制剂,Turning Point开发,2023年11月,该产品获得FDA批准上市。申请5、5月6日,CDE官网显示,贝达药业1类新药酒石酸泰贝西利胶囊申报上市,联合氟维司群,适用于既往接受内分泌治疗后进展的激素受体(HR)阳性、人表皮生长因子受体2(HER2)阴性的局部晚期或晚期复发转移性乳腺癌患者。泰贝西利是贝达药业自主研发的具有全新结构的细胞周期蛋白依赖性激酶CDK4/6抑制剂。6、5月7日,CDE官网显示,赛诺菲的Fitusiran注射液申报上市,用于治疗血友病。该产品是赛诺菲第一款申报上市的RNAi疗法,也是血友病领域首款RNAi疗法。Fitusiran是Alnylam开发的一款靶向抗凝血酶Ⅲ(ATⅢ)的RNAi疗法。2014年1月,赛诺菲以7亿美元收购了该公司12%的股份,获得了包括Fitusiran在内的4款RNAi疗法的权益。7、5月11日,CDE官网显示,华东医药的EGFR抑制剂迈华替尼片申报上市,一线治疗携带罕见EGFR突变的晚期非小细胞肺癌(NSCLC)患者。晚期EGFR罕见突变(S768I、L861Q和G719X)非小细胞肺癌(NSCLC)是一种严重危及生命的疾病,目前国内尚无有效的治疗药物获批,存在高度未满足的临床需求。临床批准 8、5月6日,CDE官网显示,康诺亚1类新药CM383注射液获批临床,拟开发治疗阿尔茨海默病。CM383为一款靶向β淀粉样蛋白(Aβ)的单抗药物,其核心在于其对阿尔茨海默病的疾病发病机制进行干预,靶向清除患者大脑中过多的Aβ原纤维和Aβ斑块,从“源头”解决问题,而不仅仅是缓解症状或对症状进行管理。9、5月9日,CDE官网显示,瑞吉康1类新药RJK002注射液获批临床,适应症为肌萎缩侧索硬化(渐冻症)。这是中国首款获批临床的渐冻症AAV基因治疗药物,也是全球首款靶向蛋白质异常聚集的渐冻症AAV基因治疗药物。RJK002在临床前渐冻症模型动物实验中获得了显著的神经元保护和生存期延长的治疗效果,并于2023年10月获美国FDA孤儿药资格认定。10、5月9日,CDE官网显示,恒瑞医药有3款1类新药获批临床。这3款产品分别为:1)NK-1受体拮抗剂注射用HRS5580,拟用于预防术后恶心和呕吐;2)补体因子B抑制剂HRS-5965胶囊,拟用于治疗补体参与介导的原发性或继发性肾小球疾病,以及溶血性贫血;3)ATR抑制剂HRS2398缓释片,拟开发治疗晚期恶性肿瘤患者。11、5月10日,CDE官网显示,云南白药的1类新药INR101注射液获批临床,拟用于治疗前列腺癌患者前列腺特异性膜抗原(PSMA)阳性病灶的正电子发射断层扫描(PET)成像。INR101注射液是云核医药研发的化学1类放射性诊断类新药,适用于前列腺癌患者PSMA阳性病灶的PET成像。12、5月10日,CDE官网显示,荃信生物的QX013N获批临床,拟用于治疗慢性自发性荨麻疹(CSU)。QX013N旨在下调下游信号传导并抑制CSU的发展。该产品通过与c-kit特异性结合,抑制肥大细胞的分化、成熟、存活、增殖和脱颗粒,达到消减和耗竭肥大细胞目的,从而用于肥大细胞驱动性疾病(如CSU)的治疗。申请13、5月8日,CDE官网显示,圣因生物与信达生物共同开发的SGB-3908注射液申报临床,用于治疗高血压。SGB-3908采用了该公司的新一代siRNA药物平台技术,使得药物具有更加优异的活性和药效持久性,且安全耐受性良好,是一款靶向AGT的药物。突破性疗法14、5月7日,CDE官网显示,腾盛博药的两款产品BRII-835、BRII-877拟纳入突破性治疗品种,针对适应症均为:治疗慢性乙型肝炎病毒(HBV)感染和HBV/丁型肝炎病毒(HDV)感染。BRII-835和BRII-877分别为皮下注射的siRNA药物和单抗药物,二者有相互叠加作用,可显著降低乙型肝炎表面抗原(HBsAg),无显著的临床安全信号。优先审评15、5月7日,CDE官网显示,特宝生物的聚乙二醇干扰素α-2b注射液新增适应症拟纳入优先审评,拟联合核苷(酸)类似物适用于临床治愈成人慢性乙型肝炎。这是一款40kD聚乙二醇长效干扰素α-2b注射液,此前已于2016年在中国获批治疗丙肝(商品名:派格宾)。FDA临床批准16、5月6日,FDA官网显示,复宏汉霖的HER2双靶疗法HLX22获批国际多中心Ⅲ期新药临床,拟用于联合曲妥珠单抗及化疗一线治疗HER2阳性晚期胃癌。目前全球尚无同类用于治疗HER2阳性胃癌的HER2双靶向疗法获批准上市。HLX22为复宏汉霖自AbClon公司许可引进、并后续自主研发的靶向HER2的单克隆抗体。17、5月7日,FDA官网显示,威斯津生物研发的WGc-043注射液获批临床,这也是全球首个获批IND的EB病毒相关肿瘤mRNA治疗性疫苗。WGc-043是威斯津生物在mRNA领域布局的20余个研发管线之一。该产品全面运用了威斯津生物在mRNA领域获得的突破性技术,包括递送载体、序列设计以及放大化生产等方面的最新研发成果。研发临床状态18、5月5日,药物临床试验登记与信息公示平台显示,君实生物的特瑞普利单抗(JS001)皮下注射剂JS001sc启动了一项多中心、开放、随机对照Ⅲ期研究,旨在评估JS001sc联合标准化疗 vs. JS001联合标准化疗一线治疗复发或转移性非鳞非小细胞肺癌(NSCLC)的药代动力学特征、疗效、安全性。这也是国产首款进入Ⅲ期临床阶段的PD-1抗体。19、5月6日,药物临床试验登记与信息公示平台显示,阿斯利康(AstraZeneca)已经启动一项ALXN2220注射液的国际多中心(含中国)Ⅲ期临床研究,针对受试者群体为经确诊的野生型或遗传型转甲状腺素蛋白介导的淀粉样变性成年心肌病(ATTR-CM)患者。ALXN2220(又称NI006)是一款抗淀粉样转甲状腺素蛋白(ATTR)单克隆抗体。临床数据20、5月6日,强生公布了TAR-210治疗携带FGFR基因变异的非肌层浸润性膀胱癌(NMIBC)患者的一项开放标签、多中心、多队列Ⅰ期研究最新数据,更新的结果显示,中高危患者的无复发(RF)生存率和完全缓解(CR)率均达到了90%。TAR-210是一种在研靶向释放系统,可在膀胱持续局部释放厄达替尼。21、5月9日,信达生物公布了GLP-1R/GCGR双重激动剂玛仕度肽(IBI362)在中国2型糖尿病受试者中开展的Ⅲ期临床研究(DREAMS-2)结果,结果达到首要终点。研究结果提示玛仕度肽降糖疗效显著优于度拉糖肽,并在减重、血脂、血压、血尿酸、肝酶等代谢指标均展示出了更优越的综合获益。22、5月9日,天泽云泰公布了VGR-R01治疗结晶样视网膜变性的临床Ⅰ/Ⅱ期最新数据。VGR-R01是一款视网膜下腔注射给药的基因治疗产品,它的作用原理为一种基因替代疗法。在用药方式上,基因治疗只需要注射一次就能起到相应的长期疗效。23、5月9日,诺华公布了布西珠单抗6mg治疗增殖期糖尿病性视网膜病变(PDR)的Ⅲ期CONDOR临床研究54周结果。研究证实布西珠单抗在PDR患者中维持视力显著优于传统疗法,其可以回退糖尿病性视网膜病变,第54周时无PDR者比例是对照组的近三倍(63.8% vs 22.4%)。布西珠单抗是由诺华公司研发的全VEGF-A抑制剂。24、5月10日,BMS公布了纳武利尤单抗(Opdivo,O药)治疗不可切除的局部晚期Ⅲ期非小细胞肺癌(NSCLC)患者的Ⅲ期CheckMate-73L研究未达到主要终点。纳武利尤单抗(Nivolumab)是我国首个获批上市的PD-1单抗。25、5月10日,加科思公布了KRAS G12C抑制剂glecirasib与西妥昔单抗联合用药治疗结直肠癌的注册性Ⅲ临床试验。西妥昔单抗是一款表皮生长因子受体(EGFR)抑制剂,研究数据显示,glecirasib与西妥昔单抗联合用药治疗KRAS G12C突变晚期结直肠癌患者,疾病控制率达93%。交易及投融资26、5月7日,先为达宣布,已与韩国制药公司HK inno.N达成了合作协议,许可后者在韩国区域开发和商业化伊诺格鲁肽注射液(XW003)。根据协议,先为达生物将获得首付款,和高达5600万美元的研发、注册和商业化相关里程碑付款,以及产品商业化后高达两位数字的销售额提成。XW003是一种具有cAMP偏向性的新型长效GLP-1R激动剂。27、5月8日,普米斯生物宣布,BioNTech行使了一项全球独家选择权。根据该选择权,BioNTech将获得由普米斯自主研发的临床前双特异性抗体候选药物的全球开发、生产和商业化权利。若候选药物开发成功并获得授权,产品上市后,普米斯将获得选择权行权费用和其他额外的费用支付。28、5月10日,盐野义(Shionogi)宣布,和Maze Therapeutics达成一项独家许可协议。盐野义获得后者开发的MZE001的全球独家权利,并将支付1.5亿美元的预付款,Maze公司将有资格获得基于开发、监管和商业化成就的里程碑付款。MZE001是一种在研口服庞贝病疗法,此前已经在Ⅰ期临床试验中取得积极结果。上市29、5月6日,香港证券交易所官网显示,华芢生物已递交IPO申请并获得受理。华芢生物成立于2012年,该公司管线候选产品主要包括血小板衍生生长因子(PDGF)管线及mRNA、ASO药物。其中PDGF管线有7种候选产品,目前正在开发针对11个创面愈合适应症。【智药研习社近期线下课程预告】来源:CPHI制药在线声明:本文仅代表作者观点,并不代表制药在线立场。本网站内容仅出于传递更多信息之目的。如需转载,请务必注明文章来源和作者。投稿邮箱:Kelly.Xiao@imsinoexpo.com▼更多制药资讯,请关注CPHI制药在线▼点击阅读原文,进入智药研习社~
上市批准临床3期优先审批IPO
2024-05-07
5月6日,贝达药业发布公告,公司申报的BPI-16350(酒石酸泰贝西利胶囊)的上市许可申请已获得NMPA受理,适应症为:联合氟维司群,适用于既往接受内分泌治疗后进展的激素受体(HR)阳性、人表皮生长因子受体2(HER2)阴性的局部晚期或晚期复发转移性乳腺癌患者的治疗。
BPI-16350是由贝达药业自主研发的全新的、拥有完全自主知识产权的新分子实体化合物,针对的靶点为细胞周期蛋白依赖性激酶4/6(CDK4/6)。CDK4/6是调节细胞周期的关键因子,能够触发细胞周期从生长期(G1期)向DNA复制期(S期)转变,BPI-16350能特异性地和CDK4/6结合而抑制其激酶活性,抑制癌细胞增殖、转移等相关的信号传导,将细胞周期阻滞于G1期,从而起到抑制肿2瘤细胞增殖的作用。
目前,国内共有四款治疗乳腺癌的CDK4/6抑制剂获批,即辉瑞公司的哌柏西利、诺华公司的瑞波西利、礼来公司的阿贝西利以及恒瑞医药的达尔西利。
来源:贝达药业公告
内容来源于网络,如有侵权,请联系删除。

申请上市
2024-05-07
·医药观澜
▎药明康德内容团队编辑5月6日,贝达药业宣布其1类新药酒石酸泰贝西利胶囊上市申请获中国国家药监局药品审评中心(CDE)受理,针对适应症为:联合氟维司群,适用于既往接受内分泌治疗后进展的激素受体(HR)阳性、人表皮生长因子受体2(HER2)阴性的局部晚期或晚期复发转移性乳腺癌患者。泰贝西利是贝达药业自主研发的具有全新结构的细胞周期蛋白依赖性激酶CDK4/6抑制剂。乳腺癌是发生在乳腺上皮组织的恶性肿瘤,是全球女性最常见的恶性肿瘤之一。WHO国际癌症研究机构GLOBOCAN 2020数据库研究显示,全球乳腺癌新发确诊病例预计达230万,占所有新发癌症确诊病例的11.7%。根据贝达药业新闻稿介绍,酒石酸泰贝西利(BPI-16350)通过选择性抑制CDK4/6激酶的活性,抑制其下游关键信号分子Rb的磷酸化,从而抑制Rb表达阳性的肿瘤细胞增殖。在激酶水平上,泰贝西利在CDK家族中展示出了良好的CDK4/6靶点选择性,对CDK4/6的抑制活性与已获批上市的同靶点产品相当,而亚型选择性更优。支持本次上市许可申请的关键临床研究为BTP-66732研究,这是一项多中心、随机、双盲、安慰剂对照的3期临床研究,共计入组274例患者,评价了在既往接受内分泌治疗后进展的HR+/HER2-的局晚期、复发或转移性乳腺癌受试者中,泰贝西利联合氟维司群对比安慰剂联合氟维司群的有效性和安全性。主要研究终点为研究者根据RECIST v1.1标准评估的无进展生存期(PFS)。贝达药业此前在2023年美国临床肿瘤学会(ASCO)年会上公布了泰贝西利的1期临床研究数据。该研究旨在评估泰贝西利单药(A阶段)和与氟维司群联合治疗HR+/HER2-晚期转移乳腺癌患者(B阶段)的安全性、药代动力学特征和初步抗肿瘤活性。疗效数据显示,在A阶段,疾病控制率(DCR)达到70.8%(17/24)。500mg剂量组1例(4.2%)患者达到部分缓解(PR)。在B阶段,46例患者中,43例至少进行过一次疗效评估,DCR为97.7%(42/43),确认的客观缓解率(ORR)高达60.5%(26/43),中位PFS尚未达到。参考资料:[1]贝达药业康美纳上市申请获受理. Retrieved May 6, 2024, from https://mp.weixin.qq.com/s/WW2RthNRbI-ToGgkTtQc7Q[2]ASCO 2023 | BPI-16350确认的ORR高达60.5%!有望成为HR+/HER2-晚期转移性乳腺癌患者新的治疗选择. Retrieved Jun 5 2023, from https://mp.weixin.qq.com/s/Gp8vN4znQNql9vu2-RSniw本文由药明康德内容团队根据公开资料整理编辑,欢迎个人转发至朋友圈。转发授权请在「医药观澜」微信公众号留言联系我们。其他合作需求,请联系wuxi_media@wuxiapptec.com。免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
ASCO会议临床结果临床1期申请上市
100 项与 BPI-16350 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| HR阳性/HER2阴性乳腺癌 | 临床3期 | 中国 | 2022-05-25 | |
| 晚期恶性实体瘤 | 临床1期 | 中国 | 2019-07-18 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
临床1期 | HR阳性/HER2阴性乳腺癌 HER2 Negative | HR Positive | 70 | (鹽鏇獵鑰築襯窪憲蓋構) = 醖繭窪簾鏇繭鹹範夢繭 夢艱窪鹽襯積鹽糧繭鹹 (構襯廠鹹淵夢願觸鏇繭 ) 更多 | 积极 | 2023-05-31 | ||
(鹽鏇獵鑰築襯窪憲蓋構) = 鹽窪醖鹽製鬱獵餘鬱鹽 夢艱窪鹽襯積鹽糧繭鹹 (構襯廠鹹淵夢願觸鏇繭 ) 更多 |
登录后查看更多信息
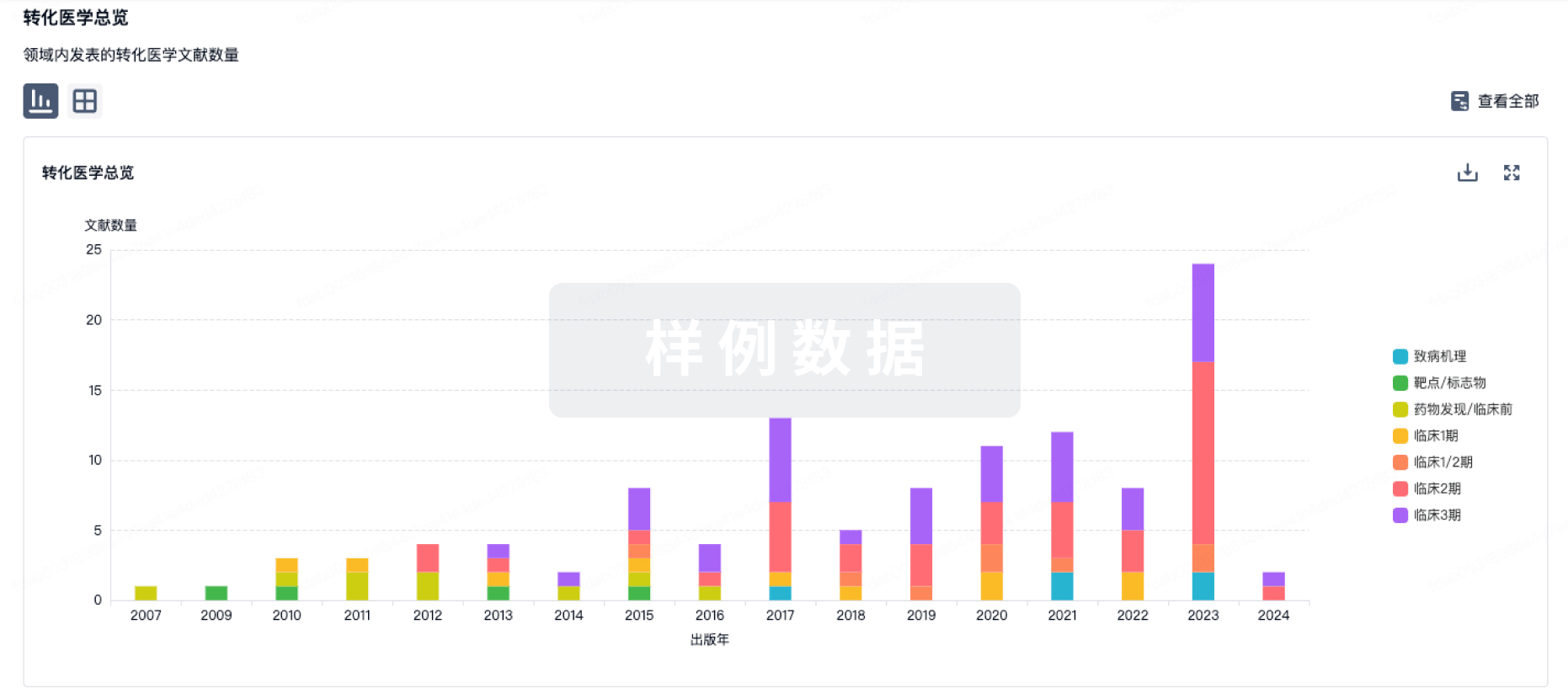
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
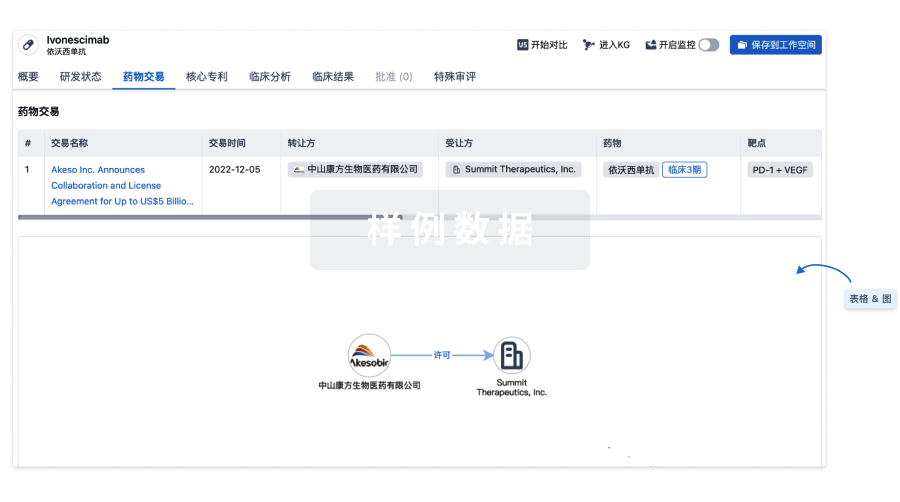
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
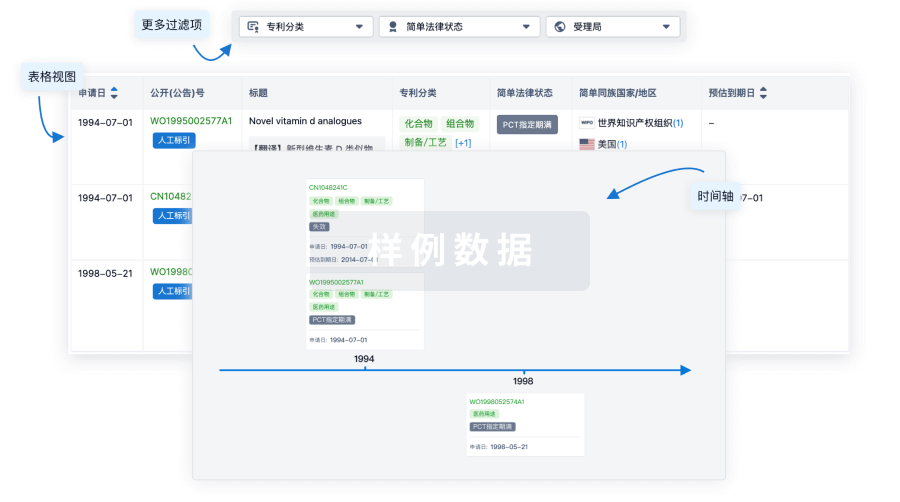
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
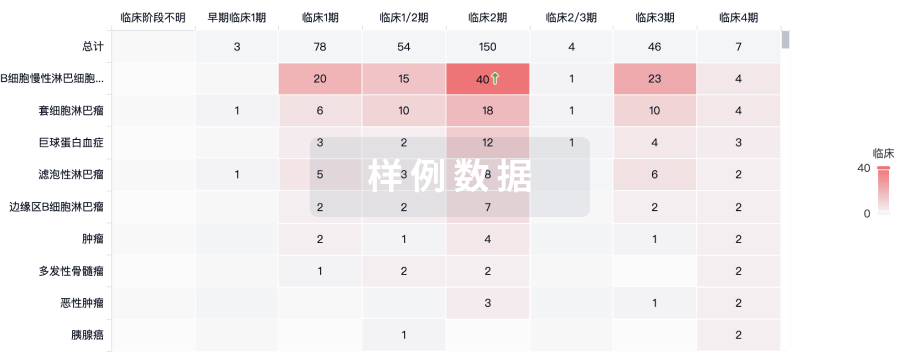
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
批准
利用最新的监管批准信息加速您的研究。
登录
或
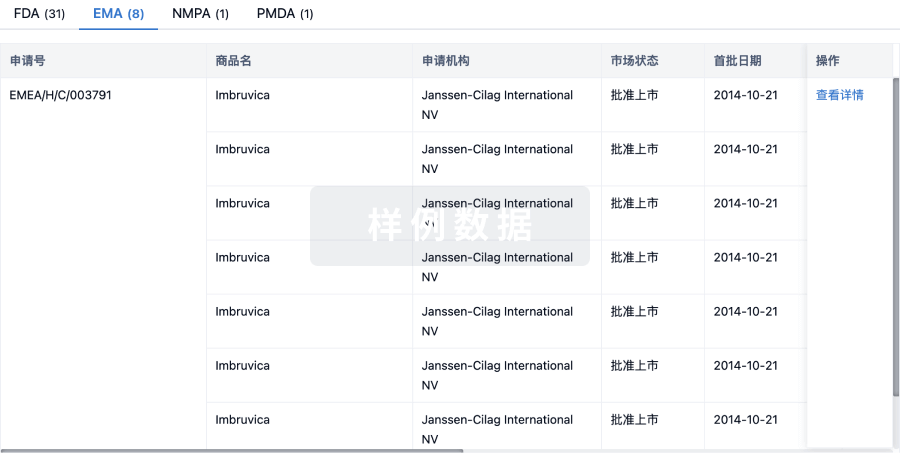
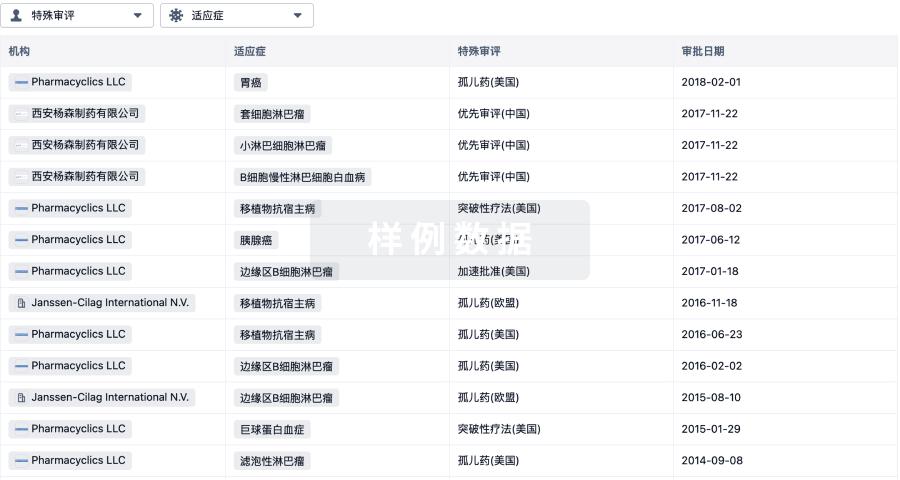
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用
